VODA
 MOLEKULA VODE
(http://www.bio.miami.edu/tom/courses/protected/MCB6/ch02/2-05.jpg)
MOLEKULA VODE
(http://www.bio.miami.edu/tom/courses/protected/MCB6/ch02/2-05.jpg)
Najbolj razširjena snov na našem planetu je voda in je zelo pomembna za vse organizme, saj jim omogoča preživetje. Tudi v celici ima voda zelo pomembno vlogo, saj predstavlja več kot 70% mase celice.
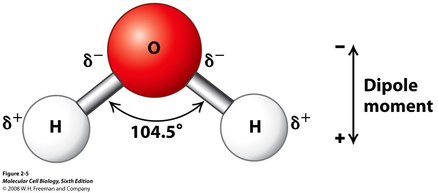
Voda je anorganska snov, ki je sestavljena iz 2 atomov vodika in iz 1 atoma kisika. Oba vodika sta s kisikom povezana s kovalentno vezjo, zato nastaneta dva vezna ali skupna elektronska para. Ker pa je kisik bolj elektronegativen, bolj privlači oba skupna elektronska para in zato se izoblikujeta pozitivni in negativni pol oziroma dipol. To pomeni, da je voda polarna molekula.
Voda je tudi topilo. Ker je voda polarna, se v njej topijo polarne snovi (oziroma topljenci). Take snovi so npr. ionske snovi, ogljikovi hidrati, vitamin C, vitamini B-kompleksa... Ne topijo pa se v njej nepolarne snovi, npr. maščobe.
Voda sodeluje tudi pri raznih kemijskih reakcijah. Poznamo dva glavna tipa kemijskih reakcij, pri katerih sodeluje voda. Prva je kondenzacija. To je kemijska reakcija, v kateri se dve manjši molekuli združita v večjo molekulo, voda pa se odcepi. Druga pa je hidroliza. To je kemijska reakcija, v kateri večja molekula razpade na dve manjši s pomočjo vode (voda vstopi in zaradi tega lahko večja molekula razpade). Primer hidrolize je npr. prebava.
Vsi vemo, da za (celično) dihanje potrebujemo kisik. Ta kisik, ki ga dihamo, pridelajo rastline (so avtotrofi) iz vode in ogljikovega dioksida. Prav voda pa je vir kisika pri fotosintezi.
Voda ima visoko specifično toploto, kar pomeni, da ji moramo dodati veliko toplote, da se segreje. To je sicer po eni strani slabo, ampak to pomeni tudi, da se počasneje ohlaja, kar pa je zelo dobro. Vsi organizmi se zato počasi segrevamo in tudi počasi ohlajamo (to nam ljudem zelo koristi v zimskem času, saj bi se drugače prej podhladili).
Sodeluje pri uravnavanju pH (kislost in bazičnost snovi).
Ima pa nekakšno "napako". Anomalija (napaka) vode je v tem, da ima največjo gostoto pri 4ºC. Posledica tega je, da voda pozimi zmrzuje od zgoraj navzdol, kar pa je zelo dobro za ribe, saj lahko na dnu preživijo čez zimo.
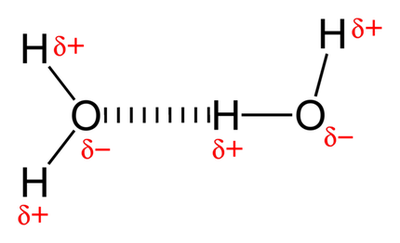
Voda ima pozitivni pol (razlaga je v drugem odstavku te strani), ki se lahko veže z negativnim polom druge molekule vode. Če se dve molekuli vode tako povežeta, nastane med njima šibka medmolekulska vez, ki ji rečemo vodikova vez. Voda pa lahko tvori različno število vodikovih vezi. V trdnem agregatnem stanju tvori 4 stalne vezi (vedno z enakimi molekulami), v tekočem agregatnem stanju 4 nestalne (vedno z drugimi molekulami vode), v plinastem agregatnem stanju pa teh vezi sploh ne tvori.
Posledica nastanka vodikovih vezi je, da ima voda obliko kapljice. Poleg tega pa so vodikove vezi vzrok, da se voda lahko dvigne po rastlini navzgor (molekule vode ustvarjajo vodikove vezi s steno in se tako dvigujejo) in je tudi vzrok, za naše znojenje (pri znojenju se ohlajamo in odvečna toplota se porabi za prekinjanje vodikovih vezi, zaradi tega pa se izloča voda).
Kozehivnost je težnja molekul vode, da ostanejo skupaj zaradi vodikovih vezi. Zaradi kozehivnosti pa ima voda površinsko napetost (gladina vode ima lastnosti prožne plošče; nekatere živali to izkoriščajo za premikanje po vodi, npr. vodni drsalec).
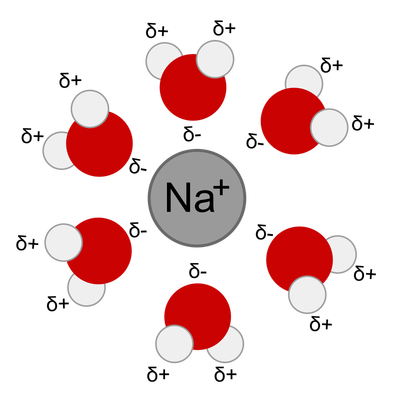
Kot že prej omenjeno voda sodeluje v kemijskih reakcijah, te vode je okrog 50% in ji pravimo metabolna voda (metabolizem=presnova). Ostali polovici vodi (50%) pa pravimo vezalna voda, saj se veže na ione ali nabite molekule. Npr. okrog natrijevega kationa pride voda, ki je proti kationu obrnjena z negativnim polom. Takrat nastane vodni ali hidratacijski ovoj.
Voda je anorganska snov, ki je sestavljena iz 2 atomov vodika in iz 1 atoma kisika. Oba vodika sta s kisikom povezana s kovalentno vezjo, zato nastaneta dva vezna ali skupna elektronska para. Ker pa je kisik bolj elektronegativen, bolj privlači oba skupna elektronska para in zato se izoblikujeta pozitivni in negativni pol oziroma dipol. To pomeni, da je voda polarna molekula.
Voda je tudi topilo. Ker je voda polarna, se v njej topijo polarne snovi (oziroma topljenci). Take snovi so npr. ionske snovi, ogljikovi hidrati, vitamin C, vitamini B-kompleksa... Ne topijo pa se v njej nepolarne snovi, npr. maščobe.
Voda sodeluje tudi pri raznih kemijskih reakcijah. Poznamo dva glavna tipa kemijskih reakcij, pri katerih sodeluje voda. Prva je kondenzacija. To je kemijska reakcija, v kateri se dve manjši molekuli združita v večjo molekulo, voda pa se odcepi. Druga pa je hidroliza. To je kemijska reakcija, v kateri večja molekula razpade na dve manjši s pomočjo vode (voda vstopi in zaradi tega lahko večja molekula razpade). Primer hidrolize je npr. prebava.
Vsi vemo, da za (celično) dihanje potrebujemo kisik. Ta kisik, ki ga dihamo, pridelajo rastline (so avtotrofi) iz vode in ogljikovega dioksida. Prav voda pa je vir kisika pri fotosintezi.
Voda ima visoko specifično toploto, kar pomeni, da ji moramo dodati veliko toplote, da se segreje. To je sicer po eni strani slabo, ampak to pomeni tudi, da se počasneje ohlaja, kar pa je zelo dobro. Vsi organizmi se zato počasi segrevamo in tudi počasi ohlajamo (to nam ljudem zelo koristi v zimskem času, saj bi se drugače prej podhladili).
Sodeluje pri uravnavanju pH (kislost in bazičnost snovi).
Ima pa nekakšno "napako". Anomalija (napaka) vode je v tem, da ima največjo gostoto pri 4ºC. Posledica tega je, da voda pozimi zmrzuje od zgoraj navzdol, kar pa je zelo dobro za ribe, saj lahko na dnu preživijo čez zimo.
Voda ima pozitivni pol (razlaga je v drugem odstavku te strani), ki se lahko veže z negativnim polom druge molekule vode. Če se dve molekuli vode tako povežeta, nastane med njima šibka medmolekulska vez, ki ji rečemo vodikova vez. Voda pa lahko tvori različno število vodikovih vezi. V trdnem agregatnem stanju tvori 4 stalne vezi (vedno z enakimi molekulami), v tekočem agregatnem stanju 4 nestalne (vedno z drugimi molekulami vode), v plinastem agregatnem stanju pa teh vezi sploh ne tvori.
Posledica nastanka vodikovih vezi je, da ima voda obliko kapljice. Poleg tega pa so vodikove vezi vzrok, da se voda lahko dvigne po rastlini navzgor (molekule vode ustvarjajo vodikove vezi s steno in se tako dvigujejo) in je tudi vzrok, za naše znojenje (pri znojenju se ohlajamo in odvečna toplota se porabi za prekinjanje vodikovih vezi, zaradi tega pa se izloča voda).
Kozehivnost je težnja molekul vode, da ostanejo skupaj zaradi vodikovih vezi. Zaradi kozehivnosti pa ima voda površinsko napetost (gladina vode ima lastnosti prožne plošče; nekatere živali to izkoriščajo za premikanje po vodi, npr. vodni drsalec).
Kot že prej omenjeno voda sodeluje v kemijskih reakcijah, te vode je okrog 50% in ji pravimo metabolna voda (metabolizem=presnova). Ostali polovici vodi (50%) pa pravimo vezalna voda, saj se veže na ione ali nabite molekule. Npr. okrog natrijevega kationa pride voda, ki je proti kationu obrnjena z negativnim polom. Takrat nastane vodni ali hidratacijski ovoj.
VIRI SLIK NA ZAČETKU STRANI
vrtnica s kapljico: http://3.bp.blogspot.com/-JzIud-DuXhY/VN2K_X8UsDI/AAAAAAAADi8/KYY00zi8wN4/s1600/flower-rose-petals-water-drop-hd-wallpaper-zoomwalls.jpg
voda: http://moneymorning.com/wp-content/blogs.dir/1/files/2013/02/water.jpg
voda pod mikroskopom: http://wordlesstech.com/wp-content/uploads/2013/02/Microscopic-Water-photography-by-Laurent-Costa-1-640x460.jpg
VIRI SLIK NA KONCU STRANI
vodikova vez: http://upload.wikimedia.org/wikipedia/commons/thumb/b/b5/Hydrogen-bonding-in-water-2D.png/640px-Hydrogen-bonding-in-water-2D.png
anomalija vode: http://h-e.si/images/8.jpg
hidratacijski ovoj: http://upload.wikimedia.org/wikipedia/commons/thumb/6/67/Na%2BH2O.svg/2000px-Na%2BH2O.svg.png
vrtnica s kapljico: http://3.bp.blogspot.com/-JzIud-DuXhY/VN2K_X8UsDI/AAAAAAAADi8/KYY00zi8wN4/s1600/flower-rose-petals-water-drop-hd-wallpaper-zoomwalls.jpg
voda: http://moneymorning.com/wp-content/blogs.dir/1/files/2013/02/water.jpg
voda pod mikroskopom: http://wordlesstech.com/wp-content/uploads/2013/02/Microscopic-Water-photography-by-Laurent-Costa-1-640x460.jpg
VIRI SLIK NA KONCU STRANI
vodikova vez: http://upload.wikimedia.org/wikipedia/commons/thumb/b/b5/Hydrogen-bonding-in-water-2D.png/640px-Hydrogen-bonding-in-water-2D.png
anomalija vode: http://h-e.si/images/8.jpg
hidratacijski ovoj: http://upload.wikimedia.org/wikipedia/commons/thumb/6/67/Na%2BH2O.svg/2000px-Na%2BH2O.svg.png